搜索


近日,上海交通大学生命科学技术学院、微生物代谢国家重点实验室冯雁团队在Nucleic Acids Research上发表题为“Argonaute integrated single-tube PCR system enables supersensitive detection of rare mutations”的文章。该工作揭示了不同高温微生物 Argonaute蛋白的核酸酶特性,发现其对单碱基突变(SNV)靶标序列精准识别的规律,发展了“一管式”PCR多重核酸富集和检测的A-Star (Ago-Directed Specific Target Enrichment and Detection)新策略,实现血液等样本中低丰度突变基因的高效、多重富集和检测。上海交通大学副研究员刘倩和博士生郭翔为该论文共同第一作者,冯雁教授为通讯作者。研究工作由上海交通大学、上海交通大学附属第一医院、仁济医院、人和未来生物科技公司等合作完成。上海交通大学转化医学中心提供研究平台支持。
.png)
对血液或体液中肿瘤细胞释放DNA片段的液体活检,凭借其无创性、敏感性、动态性等特质,可实现肿瘤早期筛查及伴随诊断。然而,由于游离核酸含量低和易降解,因此在复杂背景基因中来特异性富集和检测肿瘤基因得到广泛关注。常用的PCR等方法具有简单、省时等优点,但其检测灵敏度有限;近年来,基因编辑工具酶CRISPR/Cas在核酸检测中的应用,提升了检测灵敏度和便捷性,但Cas酶对靶标序列PAM选择性、长RNA guide合成昂贵且不稳定等问题,导致检测成本、灵敏度、多重性等方面仍存在局限性。因此,研发能特异性富集靶标序列的新型核酸酶是解决上述难题的有效途径,建立高灵敏度、多重和简便的新型核酸检测技术对于基础研究和临床应用都具有重要意义。
.png)
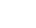
图1. “A-Star”低丰度 SNV富集和检测工作原理
论文作者在对嗜热微生物Ago蛋白的系统研究中,揭示其高温稳定性、可编程性、特异性催化活性、多重正交反应等优良特性,提出了Argonaute (Ago)核酸酶-PCR耦联的“A-Star” (Ago-Directed Specific Target Enrichment and Detection)核酸检测和富集的新策略(图1)。巧妙采用guide DNA“双点错配”设计的策略,使Ago蛋白在PCR变性步骤(94 oC)选择性剪切野生型基因,保留的突变基因可在PCR退火(~58 oC)、延伸(~72 oC)步骤中得以循环扩增,实现低丰度突变基因的超高效率富集和精准检测。研究人员对KRAS、PIK3CA和EGFR等多个肿瘤突变基因进行富集,证实A-Star能检测0.01%的低丰度突变,富集效率高达5,500倍。
.png)
图2. “A-Star”用于临床样品(A)及多重肿瘤突变(B)的富集和检测
“A-Star”在血液和实体瘤组织等复杂样品中能稳定检出靶标肿瘤基因(图2A)。考虑到实际样本中可能存在多种基因突变,通过设计多对DNA引导链,“A-Star”在单酶“一管式”反应体系中实现了多肿瘤基因的检测,且信号之间无交叉干扰(图2B)。总之,本研究所建立的“A-Star”低丰度核酸富集和检测技术,具有极高灵敏度、简便快捷及多重检测等分子检测优势,在基因诊断及遗传疾病治疗等分子生物学和医学领域具有重要应用潜力。
本研究得到了国家自然科学基金面上项目(31770078)和科技部重点研发计划(2020YFA0907700)的经费支持。
文章链接:https://doi.org/10.1093/nar/gkab274


 首页
首页

 学院概况
学院概况

 师资队伍
师资队伍

 人才培养
人才培养

 招生就业
招生就业

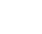 科学研究
科学研究

 平台基地
平台基地

 党群工作
党群工作

 校友之家
校友之家

 安全工作
安全工作

 网上办事
网上办事

 当前位置:
当前位置: